蛋白組/代謝組
- 定量蛋白質(zhì)組學
- DIA非標定量

- Label free非標定量

- TMT標記定量

- PRM靶向定量
- Western Blot
蛋白/核酸相互作用
- RNA-蛋白/RNA互作
- RNA pull down

- circRNA pull down

- miRNA pull down

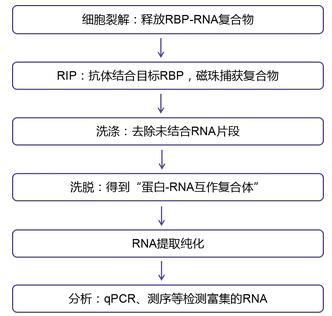
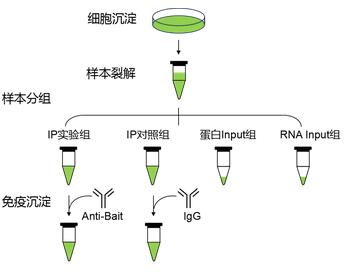
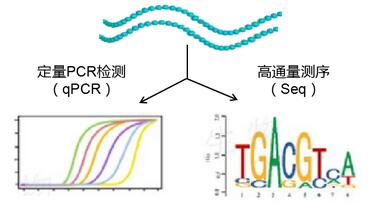
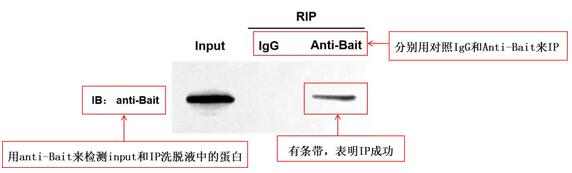
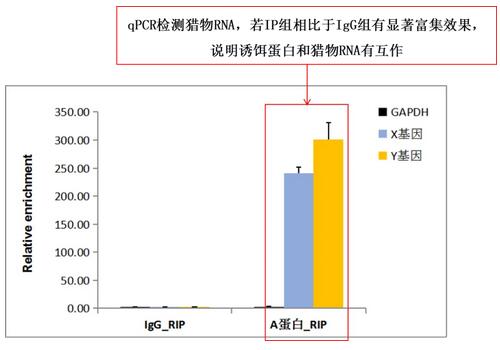
- RIP

- DNA-蛋白互作
- DNA pull down

- ChIP (染色質(zhì)免疫共沉淀)

- 化合物-蛋白互作
- 化合物pull down

細胞株構(gòu)建
- 表達細胞株
- 基因表達穩(wěn)轉(zhuǎn)株構(gòu)建(轉(zhuǎn)座子)
- 基因表達穩(wěn)轉(zhuǎn)株構(gòu)建(慢病毒)
- 抗體表達穩(wěn)轉(zhuǎn)株(CHO細胞)
- 敲除細胞株
- 基因敲除單克隆株(Crispr-cas9)
分子/細胞生物學
IP / Pull down Beads
一抗
分子互作試劑盒


 實驗熱線:4006991663
實驗熱線:4006991663